学院新闻
孔炜和孙金鹏团队发现体内血管紧张素II受体AT1的偏好性拮抗剂COMP及其在抑制腹主动脉瘤中的关键作用
2021年1月28日,北京大学JDB电子官方网站生理学与病理生理学系孔炜教授和孙金鹏教授合作,在《Cell Research》上发表了题为“Cartilage oligomeric matrix protein is an endogenousβ-arrestin-2-selective allosteric modulator of AT1 receptor counteracting vascular injury”的研究论文,首次发现内源性血管紧张素II受体AT1的偏好性抑制机制,具有重要的理论意义。

G蛋白偶联受体(GPCR)偏好性的激动或抑制可选择性地调控下游信号和相关功能,是近10年来GPCR药物开发的热点。AT1受体,属于GPCR,参与了多种重大心血管疾病的发生发展。目前已发现内源性AT1受体的偏好激动分子或因素,包括Ang1-7和机械牵张力,这些因素往往促进心血管疾病的发展,因此,体内可能也存在抑制AT1活力的内源性拮抗剂来维持血管稳态,但是否真正存在AT1受体的内源性拮抗剂尚不清楚。腹主动脉瘤是高度致死的心血管疾病,目前临床尚缺乏有效的药物治疗策略。该论文发现血管细胞外基质蛋白COMP(cartilage oligomeric matrix protein)是一种内源性AT1受体的偏好性变构调控分子,通过选择性抑制b-arrestin-2信号,进而发挥抑制腹主动脉瘤的保护作用。COMP也是我们所知的文献中第一个报道的GPCR内源性偏好性拮抗剂。人类编码800多个GPCR,是否其他GPCR也存在类似的内源性拮抗剂,来维持组织稳态,非常值得将来继续进行研究。
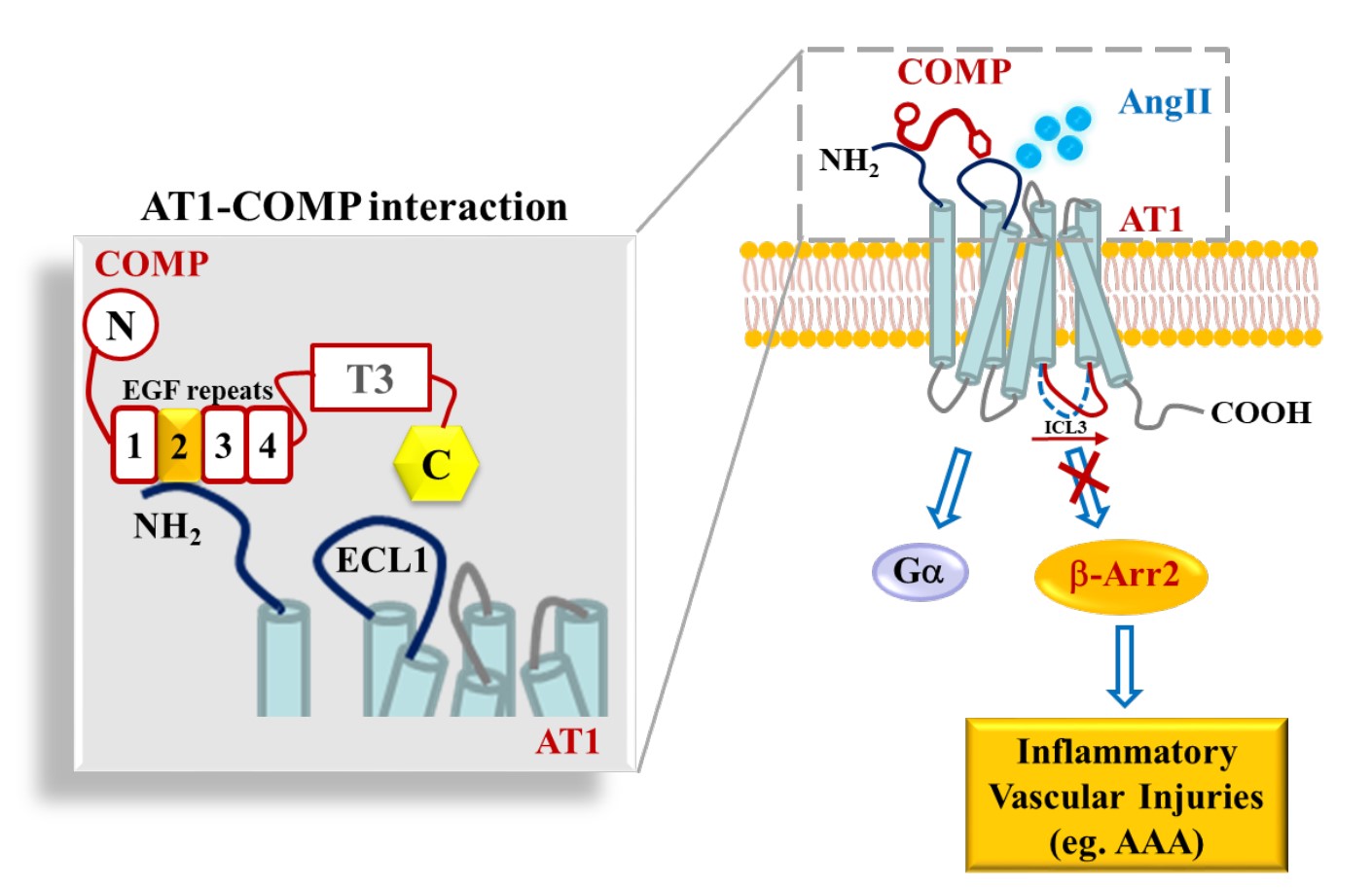
该研究首先通过病例对照试验,发现腹主动脉瘤患者血浆COMP水平显著下降,伴随腹主动脉瘤患病风险的显著增加。COMP缺陷显著加重血管紧张素II诱导的小鼠腹主动脉瘤,提示COMP具有抑制腹主动脉瘤发生与发展的保护作用。机制上,COMP缺陷并不影响血管紧张素II的产生和AT1受体的表达,但PLA、SPR、哺乳动物细胞双杂交和分子间BRET等实验,提示COMP可与AT1的N端胞外区直接结合。有趣的是,COMP并不影响AT1 下游G蛋白信号,但选择性抑制AT1-b-arrestin-2信号及其相关的AT1受体构像变化。同位素竞争结合实验表明,COMP只影响AT1/b-arrestin-2复合物的高亲和力配体结合,但不影响AT1受体本身的配体结合。这些研究结果证实COMP是AT1-b-arrestin-2信号的偏好性变构拮抗剂。COMP和AT1或COMP和b-arrestin-2的双敲小鼠,血管紧张素II诱导后的腹主动脉瘤发生率显著减少。COMP的EGF2结构域(53个氨基酸)介导了COMP与AT1受体胞外N端的结合,而在过表达EGF2模拟肽可显著抑制腹主动脉瘤的发生与发展,提示EGF2结构域具有潜在的临床转化应用意义。
北京大学JDB电子官方网站付毅副教授、北京大学第一医院黄娅茜副研究员和山东大学JDB电子官方网站杨照副教授为该论文的共同第一作者,北京大学JDB电子官方网站孔炜教授和孙金鹏教授为通讯作者。该工作还受到刘剑峰教授、王宪教授、徐清波教授、高培教授、王文恭教授和郭伟教授等的支持与合作。该项研究获得国家自然科学基金创新群体、杰出青年基金项目和国家重点研发计划的资助。
原文链接:https://doi.org/10.1038/s41422-020-00464-8

